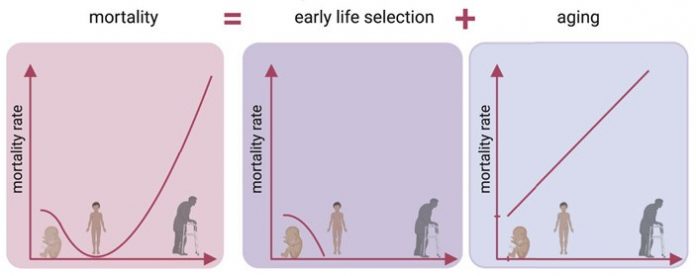
Рис. 1. Кривая смертности человека (слева) по мнению авторов новой работы раскладывается на сумму двух кривых: одна описывает естественный отбор в младенчестве (по центру), вторая — смертность «от старости» (справа). Изображение из обсуждаемой статьи в Cell Reports
На кривой смертности людей — зависимости смертности от возраста — есть «провал» в районе 9 лет. Поскольку рост смертности считается одним из критериев старения, то получается, что до 9 лет люди стареют «отрицательно», ведь смертность падает. Недавно в журнале Cell Reports вышла статья, авторы которой нашли этому феномену другое объяснение. Они полагают, что ранняя смертность — это проявление естественного отбора на неблагоприятные мутации, которая к старению не имеет никакого отношения. Таким образом, смертность человека, по их мнению, нужно рассматривать как сумму двух этих факторов, а рост смертности является не лучшим критерием старения.
Старение — непростая тема. Определенно можно сказать, что с годами она так или иначе касается каждого, и что, в частности из-за этого, ее изучению посвящены усилия многих ученых. При этом у термина «старение» до сих пор нет четкого определения. Несмотря на то, что, казалось бы, все представляют себе, что это такое, попытки дать однозначное определение заходят в тупик. Например, если сказать, что старение — это постепенное изнашивание организма, то как быть с бодрыми пожилыми людьми, которые живут активной жизнью и не жалуются на здоровье? А если, к примеру, считать старыми тех, кто потерял способность быстро ходить, то придется в ряды стариков принять и молодых инвалидов.
Поэтому мы не только не можем достоверно отличить старый организм от молодого, но и до конца не знаем, как определить, что он стареет и когда этот процесс начинается. Одним из самых широко употребимых критериев старения сегодня остается закономерность, которую еще в XIX веке вывел английский математик Бенджамин Гомперц: с возрастом увеличивается риск смерти от естественных причин (см. Распределение Гомперца). Таким образом, если какие-то организмы со временем начинают умирать чаще (растет их смертность), можно говорить о том, что они стареют.
Критерий Гомперца удобен тем, что его просто применять на любых модельных объектах. Большинство работ, которые посвящены продлению жизни, опираются именно на этот критерий, а их авторы строят для своих подопытных животных графики выживаемости, обратные к графикам смертности — то есть измеряют, какой процент от исходной популяции остается в живых в каждый момент времени (рис. 2). Сдвиг кривой вправо означает, что смертность «откладывается» на более поздний возраст, следовательно, вместе с этим тормозится и старение.
Рис. 2. Влияние рапамицина на выживаемость самцов мышей. Синий график — контрольные животные, красный — принимавшие рапамицин. По горизонтальной оси отложен возраст мышей (в днях), по вертикальной — доля живых особей. Рисунок из статьи D. E. Harrison et al., 2009. Rapamycin fed late in life extends lifespan in genetically heterogeneous mice; см. также новость Рапамицин замедляет старение у мышей («Элементы», 15.07.2009)
На каждом человеке в отдельности такой критерий применить, конечно, невозможно. Но и в целом кривая Гомперца у людей не вполне соответствует теоретической закономерности: риск умереть не растет в течение всей жизни. Так, есть подозрения, что у сверхдолгожителей (так называют людей, которые старше 105 лет; см.: Человечество приблизилось к пределу долголетия, «Элементы», 11.10.2016) кривая выходит на плато (E. Barbi et al., 2018. The plateau of human mortality: Demography of longevity pioneers), то есть риск умереть становится постоянным (рис. 3). Однако это утверждение — предмет споров, поскольку выборки сверхдолгожителей крайне малы, и результат может меняться в зависимости от методики и точности подсчетов.
Рис. 3. Предсказанное плато смертности: риск смерти (в логарифмической шкале) в зависимости от возраста. Черная линия — равномерный рост риска умереть, синий пунктир — данные по реальным долгожителям, оранжевым показан прогноз на основании данных по долгожителям. Рисунок из статьи E. Barbi et al., 2018. The plateau of human mortality: Demography of longevity pioneers
Но и с другой стороной этой кривой все не вполне гладко (в прямом смысле слова). Гомперца в свое время не особенно интересовали дети, поэтому он строил свой график, начиная с 10-летних. Тем не менее, по современным данным в начале жизни риск умереть тоже меняется неравномерно: у новорожденных смертность относительно высока, затем она падает, образуя «провал» в районе 9 лет (рис. 4), а потом снова начинает расти и уже не снижается до самого конца жизни. Этот спад, на самом деле, довольно неглубокий: риск умереть даже у новорожденных относительно невелик, поэтому, чтобы его рассмотреть, приходится строить график в логарифмической шкале — в обычной он фактически исчезает.
Рис. 4. Динамика смертности людей возрастом до 25 лет с детским «провалом» в районе 9 лет. График из статьи E. M. G. Milne, 2006. When does human ageing begin?
Тем не менее, «провал детства», в отличие от «плато старения», появляется при любых подсчетах в любой популяции, причем не только у людей, но и у других животных (см. D. Levitis, 2012. Before senescence: the evolutionary demography of ontogenesis). Если следовать определению старения как растущего риска умереть, то получается, что ранние этапы жизни соответствуют «отрицательному старению» (negative senescence), а «настоящее» старение начинается — у человека — после 9 лет.
В самом факте отрицательного старения нет ничего удивительного: известны животные, которые в этой фазе задерживаются на всю или почти всю жизнь (как, например, красноногая лягушка, см. O. R. Jones et al., 2013. Diversity of ageing across the tree of life). Тем не менее, до сих пор не было ясно, чем этот «провал детства» вызван. Можно, например, предположить, что на ранних этапах развития организм накапливает меньше повреждений (таких как мутации в ДНК или неправильно свернутые белки), потому что клетки делятся часто, и поломки распределяются по их потомкам. Следовательно, чем дальше, тем меньше удельная концентрация поломок в клетках, и тем ниже смертность.
В то же время возможны и другие объяснения: например, что 9 лет — максимально безопасный возраст для ребенка, когда он уже достаточно самостоятелен, чтобы себя не травмировать, но еще находится под присмотром родителей. Если так, то кривая смертности для людей не в полной мере соответствует старению, и рост смертности — не лучшее определение для старения.
Чтобы разобраться в том, что именно отражает «провал» на графике, группа ученых под руководством Вадима Гладышева (Vadim Gladyshev) из Гарвардской медицинской школы проверила, насколько кривая Гомперца для человека совпадает с кривыми, построенными на основе других определений старения.
Например, можно назвать старение растущим риском умереть от возрастных заболеваний. Это определение не сильно отличается от предыдущего (сводящему старение к росту смертности) — ведь за каждой смертью «от старости» на самом деле кроется смерть от конкретной болезни: в большинстве случаев даже после, казалось бы, внезапной кончины при вскрытии можно найти следы конкретной патологии. Тем не менее, для смертности от каждой возрастной болезни можно построить отдельную кривую (рис. 5). Оказалось, что кривые смертности от множества болезней, заболеваемости раком и даже посещаемости врача по форме воспроизводят общую кривую смертности. Следовательно, если понимать старение как накопление возрастных болезней, то кривая Гомперца вполне его отражает.
Рис. 5. Кривые смертности: A — от всех причин, В — от болезней сердца, сепсиса, гриппа и пневмонии и всех остальных болезней, D — кривая заболеваемости раком, Е — кривые визитов к врачу. Изображение из обсуждаемой статьи в Cell Reports
Затем ученые обратились к другому критерию старения: накоплению патогенных мутаций в клетках. Подсчитывать количество мутаций можно разными способами; в данном случае авторы работы воспользовались базой данных по опухолевым геномам и построили зависимость количества мутаций в опухоли от возраста, в котором ее обнаружили. И здесь график получился совсем не похожим на кривую Гомперца: число мутаций увеличивалось равномерно и непрерывно, начиная с первых лет жизни и до конца. Получается, что эти два определения старения противоречат друг другу: согласно мутационной теории, старение должно начинаться с первых лет (если не с первых дней жизни зародыша — нет причин считать, что в эмбриональном периоде опухоли не образуются, см.: Пренатальная диагностика опухолей у плода), а согласно Гомперцу — с 9 лет.
Рис. 6. Встречаемость мутаций в опухолевом геноме в зависимости от возраста. Слева направо: злокачественная лимфома, опухоли мягких тканей, детский рак мозга. Изображение из обсуждаемой статьи в Cell Reports
Тогда исследователи обратились к третьему способу измерить старение — эпигенетическим часам. С течением времени в человеческих клетках происходит переупаковка ДНК: часть нитей скручивается, закрывая тем самым доступ к информации, которая на них записана, а другая часть, напротив, разворачивается. Этот процесс клетка регулирует, навешивая на сами нити ДНК и гистоновые белки (на которые «намотаны» нити) эпигенетические маркеры — это химические метки, которые делают нить более «липкой» или, наоборот, более «скользкой». Соответственно, можно по набору этих меток определить возраст клеток и — с некоторой точностью — организма в целом. Наиболее широко употребимую модель эпигенетических часов — 353 участка, на которых нужно оценить наличие/отсутствие метки, — предложил в 2013 году американец Стив Хорват (S. Horvath, 2013. DNA methylation age of human tissues and cell types).
Воспользовавшись его методом, авторы обсуждаемой статьи оценили, как растет эпигенетический возраст человека, и обнаружили, что эта зависимость тоже отличается от кривой Гомперца: в начале жизни они заметили медленный рост, а дальше степень метилирования начала резко повышаться (рис. 7). Таким образом, получилось, что если верить кривым Гомперца и смертности от разных болезней, то старение начинается в 9 лет, а если опираться на мутации и эпигенетику, то — с самых первых дней жизни.
Рис. 7. Относительная степень метилирования 353 участков ДНК из «часов Хорвата» в зависимости от возраста. Изображение из обсуждаемой статьи в Cell Reports
Чтобы разрешить это противоречие, Гладышев и коллеги предположили, что ранний спад смертности вызван не отрицательным старением, а отбором на неблагоприятные мутации, то есть тем, что в раннем возрасте гибнут прежде всего носители «нерабочих» вариантов жизненно важных генов. На эту мысль их навело недавнее исследование на мышах (M. E. Dickinson et al., 2016. High-throughput discovery of novel developmental phenotypes). Ее авторы работали с мышами, нокаутными по разным ключевым генам развития (лишенными обеих копий гена). Они подсчитали смертность на разных стадиях эмбриогенеза и заметили, что она продолжает «провал детства», то есть на ранних стадиях развития выше, чем на поздних. Гладышев и коллеги построили такую же кривую для человека: у людей тоже смертность оказалась максимальной во втором триместре беременности и снизилась в несколько десятков раз за время третьего триместра.
Затем авторы обсуждаемой работы нашли среди человеческих генов ортологи тех мышиных генов, нокауты по которым приводят к смертности на разных этапах эмбриогенеза. Ученые предположили, что гомозиготы по этим генам у людей должны встречаться крайне редко, а отбор будет идти в основном по гетерозиготным мутациям. Найдя в базах данных коэффициенты селекции (параметр, который отражает силу отбора против наименее жизнеспособных особей, см. Selection coefficient) по этим генам, исследователи обнаружили, что они тоже падают в зависимости от того, на какой стадии «отсеиваются» носители неблагоприятных мутаций. Вероятно, это связано с тем, когда гены начинают работать в ходе развития: было бы логично предположить, что сила отбора, который действует на конкретный ген, тем меньше, чем позже он «включается» в течение жизни.
Таким образом, ученые предлагают рассматривать смертность как сумму двух факторов: раннего отбора на неблагоприятные мутации и возрастной смертности. Получается, что смертность в любом случае связана с мутациями, но они имеют разную природу: в начале жизни отбраковываются в основном те, что ребенок унаследовал от родителей, а в течение жизни — те, которые наряду с другими повреждениями возникли независимо в клетках взрослого организма. Эти два фактора смертности действуют в противофазе, а на 9 лет приходится минимум для их суммарного влияния: отбор уже почти закончился, а возрастная смертность еще не набрала силу.
Рис. 8. Кривая смертности как сумма двух факторов: раннего отбора и старения. Изображение из обсуждаемой статьи в Cell Reports
Из этой модели есть несколько важных следствий. Первое заключается в том, что рост смертности — не лучшее и не универсальное определение старения. И если в середине жизни закономерность, подмеченная Гомперцем, остается справедливой и никем не оспоренной, то по меньшей мере в начале жизни она неверна: ранняя смертность, судя по всему, никакого отношения к старению не имеет. Поэтому, как бы удобно ни было измерять старение риском умереть, другие критерии — например, накопление мутаций и других повреждений или изменение метилирования ДНК, — могут оказаться более корректными.
Здесь можно было бы возразить, что мы довольно редко сталкиваемся с необходимостью измерять старение маленьких детей и тем более эмбрионов (хотя и здесь есть исключения: например, ускоренно стареющие дети с прогерией Хатчинсона — Гилфорда). Тем не менее, хорошо бы, чтобы определение старения было универсальным и применимым для любых организмов на любом этапе жизненного пути. Это, в том числе, позволит нам ответить на вопрос, который до сих пор остается нерешенным: когда организм начинает стареть?
Второе важное следствие из модели Гладышева и его коллег заключается в том, что ранняя смертность, как ни парадоксально, маскирует раннее начало старения. Если верить молекулярным критериям старения — количеству мутаций или эпигенетических меток — то оно начинается еще на первых этапах эмбриогенеза. Однако на этом этапе смертность, которую провоцируют эти изменения, настолько мала, что становится незаметной на фоне смертности, вызванной отбором на унаследованные от родителей мутации.
Наконец, третье следствие состоит в том, что на физиологическом уровне никакого отрицательного старения не существует — по крайней мере, у человека. Тот спад смертности, который мы видим на кривой Гомперца, означает, что наименее жизнеспособные зародыши или новорожденные погибли, и совершенно не означает, что оставшиеся в живых стали моложе или крепче. Так ли это у других животных и можно ли все-таки найти какие-то признаки отрицательного старения у людей, еще предстоит выяснить.
Источник: elementy.ru